什么是吸收光谱?吸收光谱的应用有哪些?
吸收光谱可以用来描述各种各样技术上重要的材料的吸收情况,例如颜料、涂层、窗口和滤光器等。那么,什么是吸收光谱?吸收光谱的应用有哪些?本文进行了简单总结。
什么是吸收光谱
吸收光谱通常称为分光光度法,是以测量给定波长样品吸收的光强为基础的分析技术。分光光度法,特别是在可见和紫外谱段,是最多功能和广泛应用技术在化学和生命科学中。在可见和紫外的分子吸收光谱与通过气体、液体、固体辐射通道辐射吸收测量有关。常用波长范围在190nm至1000nm,吸收介质是常温。然而,在一些情况下(例如,在酶检测)测量温度低于或高于室温是有利的或必需的。分子或分子的一部分,可以被吸收激发的称为色基团。强烈吸收紫外或可见部分的频谱的有机色基团常常有很多化学键如C=C、C=O或C=N。
分子激发能量通常由激发态分子和另一种分子(如溶质分子)碰撞以热量(动能)耗散,这样分子返回到基态。另一种情况,激发能量以一个过程的光辐射消耗掉,被称作荧光。这两种情况下,被色基团收集过的透射光强小于入射光强。
一个受激分子可以拥有任意一组被量子力学描述的能量离散量。这些量被称作分子的“能级”。在紫外、可见分光光度法,主要的能级首先决定于电子的空间分布,被称为电子能级,和小程度的振动能级,这产生于分子的各种振动模式(例如,各种共价键的拉伸和弯曲)。
能量和吸收的波长是由电子跃迁能级间的差异决定的。可以用如下方程表示:
λ = hc/(E2-E1)
E1是分子吸收前的能级,E2是通过吸收达到的能级
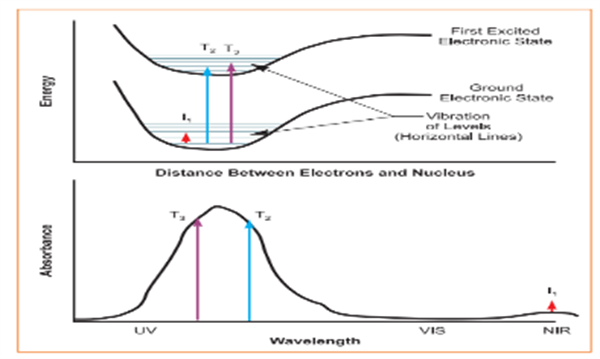
如果所有的转换都在基态的最低能级和第一激发态之间,那么吸收谱会出现窄的离散峰。然而,从一个电子能级跃迁到下一个能级可能发生在许多振动能级之间。
由于分子级的振动能级的能量差小于电子能级的最小能量差,电子跃迁由一串密间距的谱峰组成。每一个峰有和峰间距可比的显著宽度。这有峰重叠的效果,以至于一个独立的宽峰被称为电子吸收带。
对于大多数分子,吸收波长对应基态和第一激发态的任何振动能级之间的跃迁,发生在紫外和可见光范围。在一个单一的电子水平的振动能级之间的低能量转换也是可能的。这些跃迁产生红外范围内的辐射。图一展示了在能级图上的特定能量转化间的关系(上图)和吸收光谱(下图)
吸收对应波长在190nm至1000nm范围内的能量的光子的分子展示出紫外、可见吸收光谱。
处于基态或激发态的分子量化内部能量(Eint)可以被近似计算,为分析目的有足够的精度,如下(公式2):
Eint = Eel + Evib + Erot
Eel 是电子能量, Evib是振动能量,Erot是转动能量
光子吸收的结果是电子能量的变化,同时伴随振动和转动能量的变化。每一个电子振动跃迁,即一个特定电子振动跃迁,对应一个由旋转线组成的吸收带。在液体和固体中,旋转线是宽的和重叠的以至于没有旋转结构是可分辨的。
吸收光谱的应用
吸光度测量:物质浓度的测定、某些化学反应的动力学分析、材料的鉴定。
吸光度测量最通用的是用来确定物质的浓度。如果吸收系数ε已知的,并遵守比尔郎伯定律,就可以测浓度。
实际中,我们不依赖公布的ε值,因为这个量可能对试剂的制备和仪器的设计特点敏感。代替的是,它的正常做法是,从一个标准曲线得到未知样品的浓度。化学反应的进步可以允许用分光光度计测量反应物或产物随时间的浓度。这是许多酶的动力学分析基础。
最后大多数物质具有特征吸收光谱,从而可以被识别。这可以通过确定完整的频谱,并比较它在文献中发表的光谱或已知的参考图书馆的光谱。
比尔-朗伯定律
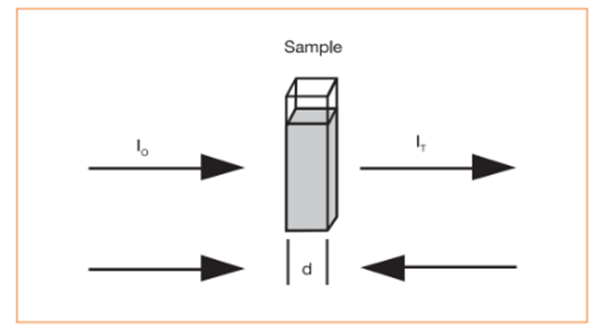
比尔-郎伯定律写给一个单独吸收体,气体的或液体的,方程如下(3):
A = -log10(IT/Io) = -εdc
IT是通过吸收介质传播过单辐射功率
I0是入射到介质上的单色功率
τi是内部的透射率(==IT/Io)
ε是摩尔吸收系数
C是物质的浓度
d是吸收路径长度
A是吸光度
内透过率τi,即透过媒介本身,不考虑边界效应,必需区分总透射率τ。不同之处在于,样品池窗的反射损耗,可以用一个参比池来补偿。
吸光度(或吸收数)α定义为α=1-τ 这里反射被认为可以忽略不计。
比尔伯朗定律只是吸收物质是彼此独立的,且在均匀介质中。
同类文章排行
- XYZ三刺激值的色度坐标和表示方法
- 色温和色调的区别是什么?
- 什么是色调?色调的分类和应用
- 12种色调的色调类型和特征分析
- 色彩基础:摄影中常用的色彩空间
- 色差空间的转换方法
- CIE1976(L*u*v*)色空间与色差公式
- 色彩管理在文物二维影像采集中的注意事项
- 色彩基础知识:色匹配函数
- 光源的温度是什么?光源的颜色温度
最新资讯文章
- 三恩时亮相CHINAPLAS 2025:火热现场
- 工厂产品色差测试工具——分光测色仪
- 色母粒色彩测量与管控
- 非接触式分光测色仪测量香料样品
- 服装、鞋类和纺织品的色彩评测
- 白度与颜色lab值区别
- 颜色lab值和黄度指数的区别
- 涂料配色案例—三恩时PeColor配色软件+TS7700分光测色仪
- 浙江三恩时诚邀您参加「2024中国国际涂料展 CHINACOAT 」
- 便携台式分光测色仪TS8450测量番茄酱的颜色
- 色差仪Lch值怎么测?色差仪Lch值的测量方法详解
- 在家叫“胖妞”,出门是测色神器——三恩时PS系列分光色差仪
- 塑料白度怎么测?塑料白度的测量方法
- 三恩时台式分光测色仪TS8560测量加德纳Gardner指数